Las ondas electromagnéticas son campos eléctricos (E) y magnéticos (H) variables, oscilantes y mutuamente perpendiculares que se desplazan por el espacio y se relacionan íntimamente con el concepto de energía

MAGNITUDES Y CUALIDADES DE LAS ONDAS

A = Amplitud de la onda (La mayor oscilación respecto de la posición de equilibrio)
c = velocidad de propagación de la onda ( cm/ seg)
l = longitud de onda ( lambda) desplazamiento del frente de onda en un ciclo (cm)
T = Período ( tiempo de un ciclo ) (seg)
n = frecuencia ( nu ) = 1/T seg –1 = ciclos/seg = Hertz
Ecuación fundamental l = c T
EL ESPECTRO CONTINUO DE ONDAS ELECTROMAGNÉTICAS
Al incidirlas ondas electromagnéticas sobre un prisma es posible separar las componentes según sus distintas frecuencias.

Algunos experimentos cruciales
a) El espectro discontinuo de emisión del Hidrógeno

Según Ridberg la frecuencia de las señales está dada por la relación:
_
n = R H ( 1 / n2 - 1 / m2 ) RH = 109.677 cm –1
n y m enteros
b) El efecto fotoeléctrico.

ECUACIÓN DE MAX PLANCK
ENERGÍA DE UN FOTÓN = h n
h = Constante de Planck = 6,62 10 -27 erg. seg
EL ATOMO DE HIDROGENO DE BOHR
(Principios Básicos de Química H.Gray)
1) Orbitas circulares
2) Momento angular = m e v r = n h / 2 p n = 1,2,3...........a
Energía asociada a los cambios de órbita
LA MECANICA CUANTICA ONDULATORIA
Efecto Compton
DUALISMO ONDA- PARTÍCULA
PRINCIPIO DE INCERTIDUMBRE DE HEISSENBERG
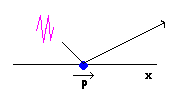
Es imposible conocer simultáneamente la posición x y el momento p de un electrón
D x D p = l . h / l = h > 0
LOS NUMEROS CUANTICOS, SU SIGNIFICADO,
SUS VALORES Y REGLAS DE COMBINACIÓN
n = Número cuántico principal.
Se asocia al tamaño y energia de los orbitales
¿Cuántos valores? infinito
¿Cuáles? 1,2 3,4,..............a ( Es el mismo n del átomo de Bohr)
l = Número cuántico secundario
Se asocia al tipo o forma de los orbitales
¿Cuántos valores? n
¿Cuáles? 0, 1, 2, 3, .........(n-1)
s p d f
Cada uno de los cuatro primeros valores se asocian respectivamente a las letras que se indican.
m = Numero cuántico magnético.
Se asocia con la orientación espacial de los orbitales
¿Cuántos valores? 2l +1
¿Cuáles? - l, - ( l-1 ), .... -1, 0, 1, ......+ ( l-1 ), + l
s = Numero cuántico de spín electrónico.
Se asocia al giro del electrón sobre su eje
¿Cuántos valores? 2
¿Cuáles? - 1 / 2 , + 1 / 2
GRÁFICOS DE ORBITALES


ATOMOS POLIELECTRÓNICOS
Ante la imposibilidad de resolver la ecuación de Schorodinger para sistemas de varios electrones, se ha supuesto y con éxito, que sucesivos electrones adoptarán los diversos modos de vibración que se encontraron para el electrón de átomo de Hidrógeno.
En palabras más simples, los sucesivos electrones se ubicaran en los orbitales ya determinados para el átomo de Hidrógeno y de acuerdo a las siguientes reglas.
Principio de exclusión de Pauli

No puede haber 2 electrones con los 4 números cuánticos iguales. Es equivalente a establecer que un orbital acepta un máximo de 2 electrones.
Principio de Estabilidad o menor Energía
Regla de Ta o de las diagonales.
Los electrones se ubican primero en los orbitales de menor energía.
Son de menor energía los de menor valor de n + l.
A igualdad de n + l se considera de menor energía los de menor n.

Principio de Hund
En el caso de varios orbitales de igual energía o "degenerados" ( igual n + l , igual n ), por ejemplo una serie de 3 orbitales p, o una serie de 5 orbitales d, o bién una de7 orbitales f. Los electrones entran de a uno en cada uno de ellos, haciéndolo primero, por convención, con spin negativo. Cuando todos los orbitales " degenerados" ya hayan recibido un electrón con spin negativo pueden formarse parejas de spines opuestos.

CONFIGURACIONES ELECTRÓNICAS Y ELECTRONES DE VALENCIA
Los electrones de valencia son aquellos que se encuentran en los orbitales de mayor número cuántico principal más aquellos que están en orbitales con el número cuántico principal anterior al mayor a condición de estar incompletos.



PokerStars Casino in New Jersey Review and Bonus Code
ResponderEliminarPokerStars Casino has a wide 용인 출장샵 variety of sports betting 익산 출장안마 options, and 양주 출장마사지 PokerStars Casino is easily one of the most prominent sportsbooks in New Jersey. 서산 출장샵 The Rating: 7/10 · Review by 남양주 출장안마 JVTECH